Mariano Esteban es elegido Presidente de la Real Academia Nacional de Farmacia
El investigador del Centro Nacional de Biotecnología del CSIC (CNB) Mariano Esteban sustituye a María Teresa Miras Portugal en la presidencia de la Real Academia Nacional de Farmacia. Y lo hace con la “ilusión de impulsar desde la Academia todo lo relacionado con el medicamento y la salud”, especialmente a través de conferencias, mesas redondas y simposios dirigidos a entender los mecanismos moleculares de la acción de los fármacos sobre el organismo.
 Durante la Sesión Inaugural del curso del pasado jueves 17 de enero, Esteban tomó posesión como nuevo presidente de la institución. Desde su nuevo cargo anima a que en una época en la que la biología avanza a pasos agigantados, se apliquen esos conocimientos “para un mayor bienestar social”.
Durante la Sesión Inaugural del curso del pasado jueves 17 de enero, Esteban tomó posesión como nuevo presidente de la institución. Desde su nuevo cargo anima a que en una época en la que la biología avanza a pasos agigantados, se apliquen esos conocimientos “para un mayor bienestar social”.
Pionero en el campo de las vacunas, caben destacar sus investigaciones en la lucha contra el sida empleando procedimientos de inmunización combinada de vectores. Sus trabajos, que están siendo financiados por distintos organismos nacionales e internacionales como la Fundación Bill y Melinda Gates, tienen aplicación en enfermedades como la hepatitis C, la gripe o el cáncer de próstata.
Para el que fuera director del CNB de 1992 a 2003, la Academia debe “fomentar el estudio de las llamadas enfermedades olvidadas”. Algo a lo que el mismo ha dedicado gran parte de su vida científica. No en vano, el propio Esteban cuenta con más de 270 artículos en revistas internacionales relacionados no solo con la producción de vacunas contra el VIH sino también contra enfermedades como la leishmaniasis o la malaria.
Para este licenciado en Farmacia (1967) y en Ciencias Biológicas (1972), la Academia “debe ser un foro donde brillen las ideas” y recalca la importancia de seguir colaborando con el sector farmacéutico ya que ambos se necesitan mutuamente.
XX Jornadas Científicas de Navidad del CNB
Descrita la estructura de la ribonucleoproteína del virus de la gripe A
Bajo la dirección de Jaime Martín-Benito y Juan Ortín, se acaba de publicar en la revista Science la estructura de las proteínas del virus de la gripe responsables de la replicación y expresión de su material genético.
 Los virus de la gripe A son endémicos en aves y también infectan al hombre y otros mamíferos, causando epidemias anuales y ocasionalmente pandemias que constituyen un grave problema sanitario. Estas epidemias ocasionan un exceso de mortalidad, generalmente en personas de avanzada edad o con su inmunidad debilitada. Además, la amenaza de pandemias de muy alta virulencia sigue siendo un peligro real, como muestran los datos de mortalidad de algunas cepas como la conocida “gripe aviar”. Estos virus de la gripe, del subtipo H5N1, no se transmiten de forma directa entre humanos, pero presentan unas tasas de mortalidad de casi el 60% (359 muertes de 608 casos registrados por la Organización Mundial de la Salud desde 2003 hasta agosto de 2012). La importancia de este patógeno también radica en el enorme impacto económico que tiene, tanto en los gastos directos sanitario-farmacéuticos como en la pérdida de decenas de millones de horas laborales en el mundo, ya que puede llegar a suponer hasta el 12% de las bajas laborables en invierno.
Los virus de la gripe A son endémicos en aves y también infectan al hombre y otros mamíferos, causando epidemias anuales y ocasionalmente pandemias que constituyen un grave problema sanitario. Estas epidemias ocasionan un exceso de mortalidad, generalmente en personas de avanzada edad o con su inmunidad debilitada. Además, la amenaza de pandemias de muy alta virulencia sigue siendo un peligro real, como muestran los datos de mortalidad de algunas cepas como la conocida “gripe aviar”. Estos virus de la gripe, del subtipo H5N1, no se transmiten de forma directa entre humanos, pero presentan unas tasas de mortalidad de casi el 60% (359 muertes de 608 casos registrados por la Organización Mundial de la Salud desde 2003 hasta agosto de 2012). La importancia de este patógeno también radica en el enorme impacto económico que tiene, tanto en los gastos directos sanitario-farmacéuticos como en la pérdida de decenas de millones de horas laborales en el mundo, ya que puede llegar a suponer hasta el 12% de las bajas laborables en invierno.
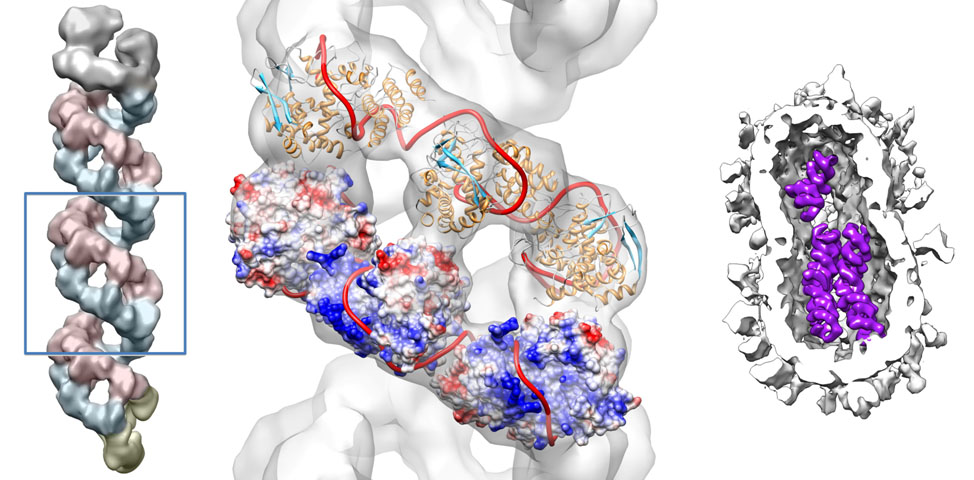
Un paso importante en el ciclo de vida del virus es la replicación y expresión de su material genético. El mensaje genético del virus está codificado en 8 segmentos de ácido ribonucleico (ARN). El ARN está unido a 4 proteínas diferentes: la polimerasa (compuesta por tres subunidades), que mantiene unidos los extremos del segmento, y múltiples copias de una misma proteína llamada nucleoproteína, que se unen al ARN como si fueran las cuentas de un collar. Esta compleja estructura es conocida como ribonucleoproteína (RNP) y funciona realmente como una máquina molecular, capaz de transcribir el mensaje genético del virus y de autoreplicarse dentro de la célula infectada para así generar la progenie de nuevos virus que infectarán otras células. El conjunto de las 8 RNPs que contienen toda la información genética del virus está empaquetado dentro de cada partícula viral de forma ordenada.
A pesar de su importancia, la información detallada de cómo se organizaban las proteínas y el ARN para generar estas RNPs era muy escasa. Por este motivo, y durante los últimos años, los laboratorios del CNB dirigidos por Juan Ortín, también investigador del CIBER de Enfermedades Respiratorias (CIBERES), y Jaime Martín-Benito han desarrollado un proyecto para la determinación de dicha estructura. La metodología de trabajo consistió en la extracción y purificación de las 8 RNPs presentes en las partículas virales, para posteriormente estudiarlas mediante técnicas de microscopía electrónica y procesamiento computacional de imágenes. Ese procedimiento permitió determinar la estructura de las RNPs aisladas y desvelar la organización de las proteínas que forman esta compleja máquina molecular. Finalmente, y usando técnicas de tomografía electrónica sobre virus intactos, se verificó que la estructura obtenida de las RNPs aisladas era la misma que la que se encontraba dentro del virus infectivo.
La estructura final obtenida muestra una organización de doble hélice con dos cadenas de ARN-nucleoproteína y la polimerasa situada en uno de los extremos del helicoide. Adicionalmente se ha verificado que dentro del virus intacto las diferentes RNPs estan dispuestas formando haces muy estrechamente empaquetados. El análisis de estos resultados, junto con los datos previos existentes, permitirá desvelar algunos de los pasos cruciales en el ciclo de vida del virus tales como los mecanismos por los que las RNPs se replican y expresan la información genética del virus, el modo en que las 8 RNPs se asocian entre sí en la partícula del virus o los mecanismos por los que los genes de virus aviares pueden transferirse a los virus humanos.
- Arranz R, Coloma R, Chichón FJ, Conesa JJ, Carrascosa JL, Valpuesta JM, Ortín J, Martín-Benito J. The structure of native influenza virion ribonucleoproteins. Science doi: 10.1126/science.1228172
¿Podemos atrapar células usando luz?
Con motivo de la Semana de la Ciencia 2012, desde el laboratorio de Nanomanipulación Óptica del IMDEA Nanociencia y del Centro Nacional de Biotecnología del CSIC, Elías Herrero Galán y Ricardo Arias González van a retransmitir vía Twitter (@CNB_CSIC) un experimeto: la captura y manipulación de células en un dispositivo de pinzas ópticas.
 La técnica de pinzas ópticas permite la captura y manipulación de partículas desde unos pocos nanómetros a centenas de micras. Mediante la aplicación de campos electromagnéticos, estas partículas no solo se pueden mover, sino que es posible medir pequeños desplazamientos en el rango de los nanómetros y fuerzas aplicadas sobre ellas en la escala de los piconewtons.
La técnica de pinzas ópticas permite la captura y manipulación de partículas desde unos pocos nanómetros a centenas de micras. Mediante la aplicación de campos electromagnéticos, estas partículas no solo se pueden mover, sino que es posible medir pequeños desplazamientos en el rango de los nanómetros y fuerzas aplicadas sobre ellas en la escala de los piconewtons.
En el Laboratorio de Nanomanipulación Óptica del IMDEA Nanociencia y del Centro Nacional de Biotecnología disponemos de un dispositivo capaz de manipular materia de esas características mediante la cofocalización de dos haces láser de igual intensidad que generan una trampa óptica simétrica.
Con el fin de comprobar si podemos emplear este aparato para realizar experimentos con células vivas, intentaremos fluir células, tanto eucariotas como procariotas, para estudiar cómo se comportan en presencia de estos campos electromagnéticos y determinar si es posible atraparlas y manipularlas sin comprometer su integridad.
El próximo miércoles día 14 de noviembre, iremos retransmitiendo el experimento en la cuenta de twitter del CNB.
Acabamos de llegar al laboratorio. Lo primero que tenemos que hacer es encender las pinzas ópticas twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012Mientras se estabiliza la temperatura de los láseres montamos la cámara de fluidos, en la que introducimos las células twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012La cámara de fluidos son dos láminas adherentes silueteadas con la forma de los canales y selladas entre dos cubres twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012La cámara de fluidos también dispone de dos tubos conectores entre canales y una micropipeta que llega al canal central twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012Colocamos la cámara entre los objetivos, fluimos tampón y alineamos dos láseres para maximizar la potencia de la trampa twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012Ya estamos listos para empezar a fluir células y tratar de atraparlas bit.ly/XEqYNT
— CNB (@CNB_CSIC) noviembre 14, 2012Empezaremos por células eucariotas, que al ser más grandes resultarán más sencillas de encontrar y de atrapar bit.ly/XEqYNT
— CNB (@CNB_CSIC) noviembre 14, 2012Disponemos de células COS-7 en cultivo, que resuspendemos y diluimos antes de fluir en la cámara de las pinzas twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012A través de una jeringa conectada a tubos de polietileno, fluimos las células en su medio de cultivo por el canal superior…
— CNB (@CNB_CSIC) noviembre 14, 2012…y esperamos que lleguen al canal central a través de uno de los tubos conectores.
— CNB (@CNB_CSIC) noviembre 14, 2012Parece que no llega ninguna célula a la zona de captura. Quizás son demasiado grandes para el diámetro del tubo...
— CNB (@CNB_CSIC) noviembre 14, 2012Vamos a probar a fluirlas directamente por el canal central, pero diluiremos un poco más para evitar tener demasiadas twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012Parece que ahora sí llegan. ¡Aquí tenemos una! Tiene un diámetro de unas diez micras twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012¡La acercamos a la trampa óptica y se atrapa! Parece que lo hace a través del núcleo, que es la zona de mayor densidad twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012No se observan efectos negativos visibles en la célula después de un tiempo en la trampa, aunque es imposible saber qué pasa en su interior
— CNB (@CNB_CSIC) noviembre 14, 2012La soltamos y la volvemos a atrapar sin aparente daño
— CNB (@CNB_CSIC) noviembre 14, 2012Ahora vamos a tratar de arrastrarla hasta la pipeta twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012Hemos podido traerla hasta la pipeta sin dificultad. Veamos si somos capaces de succionarla...
— CNB (@CNB_CSIC) noviembre 14, 2012Perfecto. La célula ha quedado inmovilizada en la pipeta sin problemas y sin sufrir deformación de su membrana twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012Con la célula inmovilizada en la pipeta ahora podríamos aproximarle sustratos con la trampa y estudiar su comportamiento mecánico
— CNB (@CNB_CSIC) noviembre 14, 2012Veamos ahora qué sucede con células procariotas, más pequeñas. Pero primero hay que fluir agua en la cámara para limpiarla
— CNB (@CNB_CSIC) noviembre 14, 2012La celda está lista para un nuevo experimento, pero antes vamos a hacer una pausa para comer. Nos vemos en media hora twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012De vuelta a las pinzas twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012Disponemos de un cultivo en medio líquido de Escherichia coli, que diluiremos como hemos hecho antes para las COS-7 twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012Fluimos ahora las bacterias directamente por el canal central
— CNB (@CNB_CSIC) noviembre 14, 2012Aquí llega una. Le aproximamos la trampa… ¡y la atrapamos sin problemas! bit.ly/UGpmgt
— CNB (@CNB_CSIC) noviembre 14, 2012En este caso, la bacteria se orienta en la dirección de propagación del láser, como si cada haz atrapara un extremo twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012¡Vaya! La bacteria es demasiado pequeña para succionarla con la pipeta, pero ¿podremos orientarla desplazando un haz con respecto del otro?
— CNB (@CNB_CSIC) noviembre 14, 2012Lentamente, desplazamos un haz láser lateralmente… ¡y vemos cómo la bacteria se orienta en esa dirección! twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012Podemos orientar la bacteria a nuestro antojo tanto en vertical como en horizontal desplazando el láser twitter.com/CNB_CSIC/statu…
— CNB (@CNB_CSIC) noviembre 14, 2012Tampoco se observa ningún daño aparente en la bacteria tras un tiempo en la trampa
— CNB (@CNB_CSIC) noviembre 14, 2012Interesantes resultados... Ahora toca repetirlos durante la tarde con diferentes células para ver si se reproduce el mismo comportamiento
— CNB (@CNB_CSIC) noviembre 14, 2012Es todo. Esperamos que os haya resultado interesante. Nosotros, a seguir trabajando
— CNB (@CNB_CSIC) noviembre 14, 201220th Anniversary Workshop
Aprovechando el vigésimo aniversario de la inauguración del Centro Nacional de Biotecnología del CSIC (CNB), el viernes 30 de noviembre de 2012 se celebra una jornada científica abierta a todo el mundo.
Participarán algunos de los miembros del Comité Científico Asesor del CNB: Maarten Koorneeff, Anna Tramontano y el premio Rey Jaime I de Protección del Medio Ambiente de 2012 Juan Luis Ramos. Además de contar con investigadores de nuestro centro como Ana C. Carrera, Juan Ortín y Salomé Prat, tendremos como ponentes a Óscar Llorca y a Manuel Serrano, destacados científicos que en su día trabajaron en el CNB.
A la presentación de la Jornada asistirá el Presidente del CSIC, Emilio Lora-Tamayo y el Rector de la Universidad Autónoma de Madrid, José María Sanz.

La Batalla de los Escarabajos
 Las claves de la evolución de las especies son la variación que hay entre los organismos de una misma especie, la selección que la naturaleza hace de los individuos y el tiempo, mucho tiempo.
Las claves de la evolución de las especies son la variación que hay entre los organismos de una misma especie, la selección que la naturaleza hace de los individuos y el tiempo, mucho tiempo.
Para estudiar cómo las especies cambian con el tiempo, un grupo de biólogos está estudiando una población de escarabajos de la especie Ovalis glucosi. Aunque desde que se conoce a estos escarabajos su color es azul, hace ya unos años se ha observado que cada vez hay más individuos de color rojo. Los científicos piensan que si son capaces de comprender el motivo por el que está ocurriendo este cambio, van a aprender un montón sobre cómo evolucionan las especies.
A los escarabajos O. glucosi les encanta guardar su comida en un agujero que excavan en el suelo. Durante varios días van recogiendo todo el alimento que se encuentran y lo guardan en su guarida. De este modo, pueden pasarse varios días sin tener que buscar nada. Bajan a comer cuando tienen hambre y descansan al sol tapando el agujero de su despensa. Como podemos imaginar, tapar la entrada del túnel es importantísimo si quieren impedir que venga otro escarabajo y les quite su comida...
Pero claro, cuando un escarabajo ve a otro quieto tomando el sol, se acerca para ver qué está escondiendo. El que está protegiendo su comida entra en su túnel y tapa con su cuerpo el agujero. Empieza entonces una pelea terrible por ver quien se hace dueño de todo lo que hay en el fondo del agujero.
Los dos escarabajos se empiezan a empujar con todas sus fuerzas hasta que uno de ellos aplasta al otro y gana la batalla. Una batalla cuyo premio es la comida que hay guardada en el fondo del túnel.
A los biólogos les ha parecido que los escarabajos rojos son un poco más fuertes que los azules. Y piensan que como ganan más veces en sus peleas consiguen más comida. Esa podría ser la explicación de que cada vez haya más escarabajos rojos y cada vez menos azules.
Pero para demostrarlo tienen que hacer un experimento. Y nosotros podemos echarles una mano.
Divididos en equipos, el profesor tiene que repartir en dos bolsas de plástico diez escarabajos rojos y diez azules (en realidad son chocolates tipo Lacasitos o M&Ms).
 Para averiguar cuales son más fuertes, si los rojos o los azules, los alumnos tienen que colocarlos en parejas y apretar con los dedos hasta que noten que uno de ellos se ha roto.
Para averiguar cuales son más fuertes, si los rojos o los azules, los alumnos tienen que colocarlos en parejas y apretar con los dedos hasta que noten que uno de ellos se ha roto.
Para cada una de las parejas de escarabajos hay que anotar cuál se rompió primero, si el rojo o el azul. En el caso de que los dos estén rotos se apuntará el que esté más roto de los dos.
Una vez que hayan terminado todos los grupos, hay en poner en común los resultados obtenidos y sumar los números de todos y cada una de las parejas.
- ¿Por qué creéis que es importante considerar los resultados de toda la clase y no sólo los de un grupo?
- ¿Hay alguna relación entre el color y la fuerza de los escarabajos? De acuerdo con los datos obtenidos, ¿podemos decir que alguno de los dos tipos de escarabajos consigue más comida?
- ¿Encuentras explicación al hecho de que haya cada vez más escarabajos rojos?
- ¿Podrán llegar a desaparecer algún día los escarabajos azules?
Esta práctica nos la enseñó Mary Colvard, profesora del Cobleskill-Richmondville High School de Cobleskill, Nueva York (Estados Unidos) y está basada en la observación de que los M&Ms de color rojo son un poco más duros que los de color azul. Si te interesa, esta práctica dirigida a alumnos de 3º y 4º de Primaria se puede descargar en pdf (1,17 MB).

Silencio por favor, infección en marcha
Aunque las plantas carecen de un sistema inmune similar al de los vertebrados, hay claras evidencias de su capacidad de defenderse de las infecciones virales a través de un mecanismo llamado silenciamiento de ARN que también está presente en hongos, vertebrados e invertebrados. En esta ruta se produce la interacción de ARNs de pequeño tamaño (entre 20 y 30 nt) con un complejo proteico capaz de dirigir la degradación, inhibición traduccional o modificaciones epigenéticas en un ARN mensajero complementario de forma específica de secuencia.
 Las interacciones entre los virus y las células hospedadoras suponen un continuo esfuerzo en ambos organismos por dar un paso más en cada batalla de su “lucha diaria”. Para superar la defensa antiviral mediada por el silenciamiento de ARN, los virus que infectan tanto plantas como otros organismos, han evolucionado desarrollando proteínas capaces de suprimir este sistema. La proteína VP3 del virus de la bursitis infecciosa (IBDV por sus siglas en inglés) es la última en ser incluida en la lista tras el trabajo presentado en la revista Plos One por los grupos de los investigadores del Centro Nacional de Biotecnología del CSIC (CNB) Juan Antonio García y José Francisco Rodríguez.
Las interacciones entre los virus y las células hospedadoras suponen un continuo esfuerzo en ambos organismos por dar un paso más en cada batalla de su “lucha diaria”. Para superar la defensa antiviral mediada por el silenciamiento de ARN, los virus que infectan tanto plantas como otros organismos, han evolucionado desarrollando proteínas capaces de suprimir este sistema. La proteína VP3 del virus de la bursitis infecciosa (IBDV por sus siglas en inglés) es la última en ser incluida en la lista tras el trabajo presentado en la revista Plos One por los grupos de los investigadores del Centro Nacional de Biotecnología del CSIC (CNB) Juan Antonio García y José Francisco Rodríguez.
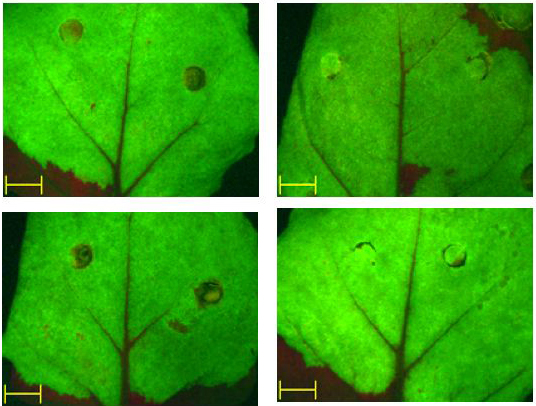
En este estudio, se ha utilizado un sistema heterólogo que permite la expresión de la proteína VP3 de IBDV en plantas de la especie Nicotiana benthamiana. En primer lugar se determinó que esta proteína es capaz de unirse no sólo al ARN genómico del virus, formado por una molécula de ARN de doble banda, sino también a ARNs pequeños, de 21 y 26 nucleótidos (nt) como los implicados en el silenciamiento mediado por ARN. Una vez expresada en plantas, VP3 es capaz de inhibir la degradación del ARN mensajero de la proteína verde fluorescente (GFP) mediada por silenciamiento de ARN que tiene lugar en las plantas control, de manera similar a la proteína NS1 del virus de la gripe y la proteína P1b del virus causante del amarilleo del melón (CVYV). Las mutaciones en las regiones implicadas en la interacción entre el ARN de doble banda y VP3 (especialmente la región Patch1) también eliminan la capacidad de la proteína de suprimir el silenciamiento por ARN, apoyando la idea de que VP3 utiliza su capacidad de unir ARN de doble banda para suprimir el silenciamiento. Además, no sólo la proteína VP3 de IBDV, sino otras proteínas de virus de la misma familias, Birnaviridae, que infectan a peces e insectos (IPVN y DXV respectivamente) son capaces de unir ARNs de doble banda y de suprimir el silenciamiento en plantas. La conservación funcional entre estas proteínas, a pesar de las diferencias en la secuencia aminoacídica sugieren que el silenciamiento mediado por ARN puede tener un papel importante no sólo en plantas, sino también en infecciones virales de peces y aves.
- Valli A, Busnadiego I, Maliogka V, Ferrero D, Castón JR, Rodríguez JF, García JA. The VP3 factor from viruses of Birnaviridae family suppresses RNA silencing by binding both long and small RNA duplexes. PLoS ONE 7(9): e45957
Presentado en el CNB el curso de la UEM de Experto en Biotecnología: Transferencia Tecnológica y Gestión de la Innovación
6º Ciclo de Seminarios Júnior 2012-2013
El 6º Ciclo de Seminarios Júnior organizados por los estudiantes predoctorales del CNB tendrá lugar los viernes a las 12:00 en el Salón de Actos del Centro Nacional de Biotecnología del CSIC a lo largo del curso 2011 - 2012.
Como se puede ver, la conferencia inaugural correrá a cargo de la investigadora del Max Plank Institute of Molecular Plant Physiology Franzisca Krajinski.
COOKIES POLICY
A cookie is a text file that is stored on your computer or mobile device via a web server and only that server will be able to retrieve or read the contents of the cookie and allow the Web site remember browser preferences and navigate efficiently. Cookies make the interaction between the user and the website faster and easier.
General information
This Website uses cookies. Cookies are small text files generated by the web pages you visit, which contain the session data that can be useful later in the website. In this way this Web remembers information about your visit, which can facilitate your next visit and make the website more useful.
How do cookies?
Cookies can only store text, usually always anonymous and encrypted. No personal information is ever stored in a cookie, or can be associated with identified or identifiable person.
The data allow this website to keep your information between the pages, and also to discuss how to interact with the website. Cookies are safe because they can only store information that is put there by the browser, which is information the user entered in the browser or included in the page request. You can not run the code and can not be used to access your computer. If a website encrypts cookie data, only the website can read the information.
What types of cookies used?
The cookies used by this website can be distinguished by the following criteria:
1. Types of cookies as the entity that manages:
Depending on who the entity operating the computer or domain where cookies are sent and treat the data obtained, we can distinguish:
- Own cookies: are those that are sent to the user's terminal equipment from a computer or domain managed by the editor itself and from which provides the service requested by the user.
- Third party cookies: these are those that are sent to the user's terminal equipment from a machine or domain that is not managed by the publisher, but by another entity data is obtained through cookies.
In the event that the cookies are installed from a computer or domain managed by the editor itself but the information collected by these is managed by a third party can not be considered as party cookies.
2. Types of cookies as the length of time that remain active:
Depending on the length of time that remain active in the terminal equipment can be distinguished:
- Session cookies: cookies are a type designed to collect and store data while the user accesses a web page. Are usually used to store information that only worth preserving for the service requested by the user at any one time (eg a list of products purchased).
- Persistent cookies: cookies are a type of data which are stored in the terminal and can be accessed and treated for a period defined by the head of the cookie, and can range from a few minutes to several years.
3. Cookies types according to their purpose:
Depending on the purpose for which the data are processed through cookies, we can distinguish between:
- Technical cookies: these are those that allow the user to navigate through a web page or application platform and the use of different options or services it exist as, for example, control traffic and data communication, identify the session, access to restricted access parts, remember the elements of an order, make the buying process an order, make an application for registration or participation in an event, use security features while browsing store content for dissemination videos or sound or share content via social networks.
- Customization cookies: these are those that allow the user to access the service with some general characteristics based on a predefined set of criteria in the user terminal would eg language, the type of browser through which you access the service, the locale from which you access the service, etc.
- Analysis cookies: they are those that allow the responsible for them, monitoring and analyzing the behavior of users of the web sites that are linked. The information gathered through such cookies are used in measuring the activity of web sites, application or platform and for the profiling of user navigation of such sites, applications and platforms, in order to make improvements function data analysis how users use the service.
Management tool cookies
This Website uses Google Analytics.
Google Analytics is a free tool from Google that primarily allows website owners know how users interact with your website. Also, enable cookies in the domain of the site in which you are and uses a set of cookies called "__utma" and "__utmz" to collect information anonymously and reporting of website trends without identifying individual users..
For statistics of use of this website use cookies in order to know the level of recurrence of our visitors and more interesting content. This way we can concentrate our efforts on improving the most visited areas and make the user more easily find what they are looking for. On this site you can use the information from your visit for statistical evaluations and calculations anonymous data and to ensure the continuity of service or to make improvements to their websites. For more details, see the link below privacy policy [http://www.google.com/intl/en/policies/privacy/]
How to manage cookies on your computer: disabling and deleting cookies
All Internet browsers allow you to limit the behavior of a cookie or disable cookies within settings or browser settings. The steps for doing so are different for each browser, you can find instructions in the help menu of your browser.
If you decline the use of cookies, since it is possible thanks to the preferences menu of your browser or settings, reject, this website will continue to function properly without the use of the same.
Can you allow, block or delete cookies installed on your computer by setting your browser options installed on your computer:
- For more information about Internet Explorer click here.
- For more information on Chrome click here.
- For more information about Safari click here.
- For more information about Firefox click here.
Through your browser, you can also view the cookies that are on your computer, and delete them as you see fit. Cookies are text files, you can open and read the contents. The data within them is almost always encrypted with a numeric key corresponding to an Internet session so often has no meaning beyond the website who wrote it.
Informed consent
The use of this website on the other hand, implies that you paid your specific consent to the use of cookies, on the terms and conditions provided in this Cookies Policy, without prejudice to the measures of deactivation and removal of cookies that you can take, and mentioned in the previous section.

 La Universidad Europea de Madrid ha presentado en el Centro Nacional de Biotecnología del CSIC (CNB) su nuevo Curso de Experto en Biotecnología: Transferencia Tecnológica y Gestión de la Innovación con la presencia de la Dra. Regina Revilla, Presidenta de ASEBIO y Directora de Relaciones Externas y Comunicación de MSD, Rocío Royo, Chief Business Officer de Amadix, Isabel García Carneros, Secretaría General de ASEBIO y José María Valpuesta, Director del CNB.
La Universidad Europea de Madrid ha presentado en el Centro Nacional de Biotecnología del CSIC (CNB) su nuevo Curso de Experto en Biotecnología: Transferencia Tecnológica y Gestión de la Innovación con la presencia de la Dra. Regina Revilla, Presidenta de ASEBIO y Directora de Relaciones Externas y Comunicación de MSD, Rocío Royo, Chief Business Officer de Amadix, Isabel García Carneros, Secretaría General de ASEBIO y José María Valpuesta, Director del CNB.