Roberto Vázquez, investigador del CIB-CSIC, destaca de sus resultados: “esta proteína posee actividad enzimática de la variedad muramidasa, y es capaz de degradar las cadenas de glicanos del peptidoglicano de la pared celular bacteriana. Este trabajo también ha identificado los aminoácidos específicos implicados en esta actividad catalítica.”
Por otro lado, Mateo Seoane-Blanco, investigador del CNB-CSIC llevó a cabo la cristalización de la proteína y su estructura utilizando la línea de cristalografía de rayos X BM13-XALOC del sincrotrón ALBA de Barcelona. “La novedad en la estructura de Pae87 es que, aunque su estructura general es similar a otras endolisinas, carece de un dominio de unión a la pared celular” destaca Seoane-Blanco. Para van Raaij, “un experimento sencillo pero elegante como incubar la enzima con peptidoglicano purificado y cristalizar la mezcla resultante, proporciona datos extra de la situación fisiológica real, en la que la endolisina interacciona con un fragmento de peptidoglicano”. Esta estructura compleja reveló que dentro del propio dominio catalítico, Pae87 tiene una región de unión a sustrato separada. Esta región se conserva en otras endolisinas similares que carecen de un dominio adicional de unión a la pared celular, pero no entre las que contienen dicho módulo y, por lo tanto, puede cumplir una función evolutiva compensatoria.
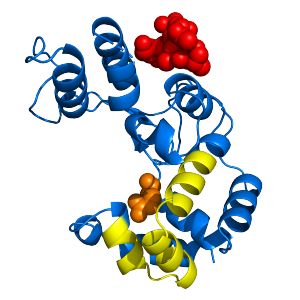
El grupo del CIB-CSIC también descubrió que la endolisina Pae87 actúa sobre las membranas de bacterias Gram-negativas, ya que posiblemente, al introducirse en la membrana provoca cambios que afectan a la viabilidad celular. Sus datos muestran que la región peptídica llamada P87 (en amarillo en la figura adjunta) cerca del final de la proteína exhibe una potente actividad antibacteriana por si misma.
Estos resultados abren el camino para futuros esfuerzos para diseñar y obtener antimicrobianos basados en endolisinas de fagos, no solo modificando las enzimas completas, sino también derivando pequeños péptidos antimicrobianos a partir de su estructura.
Referencia científica
Monomodular Pseudomonas aeruginosa phage JG004 lysozyme (Pae87) contains a bacterial surface-active antimicrobial peptide-like region and a possible substrate-binding subdomain. Roberto Vázquez, Mateo Seoane-Blanco, Virginia Rivero-Buceta, Susana Ruiz, Mark J. van Raaij, and Pedro García (2022), Acta Crystallographica section D, volume 78, pages 435-454, doi.org/10.1107/S2059798322000936