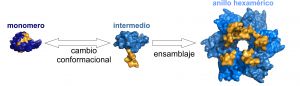
El trabajo, publicado en Nature Communications, demuestra el potencial de los interruptores alostéricos, utilizando como modelo el inhibidor de quimotripsina 2 de la semilla de cebada (CI2). Esta proteína, un inhibidor de proteasas que protege a la semilla de ser digerida, es una pequeña proteína monomérica que no oligomeriza de manera natural. Los investigadores, mediante técnicas de ingeniería de proteínas, han introducido cambios en la secuencia de aminoácidos que producen la formación de oligómeros (formando anillos simétricos de 6 y 12 subunidades) a través de un paso extra de control: un cambio conformacional que actúa como interruptor que permite controlar de manera externa cómo y cuándo la proteína oligomeriza. Luis Alberto Campos, co-autor del trabajo explica que “este sistema modelo va a servir como base para obtener proteínas funcionales con control alostérico de la oligomerización, con posibles aplicaciones en ingeniería protéica, nanotecnología y biología sintética”.
El uso de estos sistemas de modulación de las transiciones entre monómero y oligómero aporta un mayor control, dinamismo y estabilidad en la formación de complejos macromoleculares y tiene aplicaciones en nuevos proyectos de investigación como la formación de anillos que interaccionen con otras moléculas, como metales o ácidos nucleicos, o el control en la formación de poros de membrana creados por péptidos antimicrobianos mediante proteínas de fusión.
Más información:
Engineering protein assemblies with allosteric control via monomer fold-switching. Campos LA, Sharma R, Alvira S, Ruiz FM, Ibarra-Molero B, Sadqi M, Alfonso C, Rivas G, Sanchez-Ruiz JM, Romero Garrido A, Valpuesta JM, Muñoz V. Nat Commun. 2019 Dec 13;10(1):5703. doi: 10.1038/s41467-019-13686-1